- Umj.com.ua
- Ліки
- Засоби, що впливають на сечостатеву систему та статеві гормони
- Протимікробні та антисептичні засоби, що застосовуються в гінекології
- Протимікробні та антисептичні засоби, що застосовуються в гінекології, за виключенням комбінованих препаратів, які містять кортикостероїди
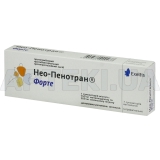
- Нео-Пенотран® форте супозиторії вагінальні блістер, №7
Нео-Пенотран® форте супозиторії вагінальні блістер, №7
- Форма випуску супозиторії вагінальні
- Кількість штук в упаковці 7 шт
- Виробник Зентіва
- Сертифікат UA/5477/01/01 від 10.11.2016
Нео-Пенотран® форте інструкція із застосування
Склад і форма випуску
действующие вещества: метронидазол и миконазола нитрат; 1 суппозиторий содержит 750 мг метронидазола и 200 мг миконазола нитрата; вспомогательные вещества: витепсол. Cупозитории вагинальные. Основные физико-химические свойства: суппозитории эллипсоидные от белого до желтоватого цвета. Противомикробные, противопротозойные, противогрибковые средства. Код АТС G01A F20. Фармакодинамика. Нео-Пенотран® Форте содержит миконазола нитрат с противогрибковым и метронидазол с антибактериальным и антитрихомонадным действием. Миконазола нитрат является противогрибковым средством, синтетическим производным имидазола, обладает широким спектром активности и особенно эффективен против патогенных грибов, включая Candida albicans. Кроме того, миконазола нитрат эффективен против грамположительных бактерий. Миконазол проявляет свое действие через синтез эргостерола в цитоплазматической мембране. Миконазола нитрат меняет проницаемость грибковой клетки видов Candida и угнетает утилизацию глюкозы in vitro. Метронидазол, 5-нитроимидазольное производное, является противопротозойным и антибактериальным средством; он эффективен против нескольких инфекций, вызванных анаэробными бактериями и простейшими, такими как Trichomonas vaginalis, Gardnerella vaginalis, и анаэробными бактериями, включая анаэробные стрептококки. Миконазола нитрат и метронидазол не имеют синергических и антагонистических эффектов. Частота клинического излечения, которое было достигнуто в открытом, многоцентровом, неконтролируемом клиническом исследовании эффективности и безопасности препарата Нео-Пенотран® Форте, при 7-дневном лечении 104 пациентов с клиническим/микробиологическим диагнозом вагинита составляла 96,6% при кандидозном вульвовагините, 98,1% при бактериальном вагинозе, 97,3% при трихомонадном вагините и 98,5% при смешанных вагинальных инфекциях. Частота микробиологического излечения составила 89,8%, 96,2%, 100%, 91,7% для каждого вида инфекции соответственно. В рандомизированном, открытом, сравнительном исследовании эффективности, безопасности и переносимости препарата Нео-Пенотран® Форте частота клинического и микробиологического излечения составляла 84% и 76% соответственно. Фармакокинетика. Абсорбция Миконазола нитрат. Абсорбция миконазола нитрата при интравагинальном введении очень низкая (примерно 1,4% от дозы). После интравагинального введения препарата Нео-Пенотран® Форте миконазола нитрат в плазме крови не определялся. Метронидазол. Биодоступность метронидазола при таком пути введения составляет 20% по сравнению с пероральным путем введения. Постоянный уровень метронидазола в плазме составлял от 1,1 до 5,0 мкг/мл после суточного интравагинального введения препарата Нео-Пенотран® Форте. Распределение Миконазола нитрат. Связывание с белками плазмы составляет 90%-93%. Его проникновение в спинномозговую жидкость низкое, но он широко распространяется в других тканях. Объем распределения составляет 1400 л. Метронидазол. Проникает в ткани и жидкости тела, включая желчь, кости, грудь, молоко, церебральные абсцессы, спинномозговую жидкость, печень и печеночные абсцессы, слюну, семенную жидкость и вагинальный секрет, и достигает концентраций, подобных таковым в плазме. Он проникает через плацентарный барьер и быстро проникает в кровоток плода. Связывание с белками плазмы не более 20%. Объем распределения составляет 0,25–0,85 л/кг. Биотрансформация Миконазола нитрат. Метаболизируется в печени. Определяются два неактивных метаболита (2,4-дихлорофенил-1 H имидазол этанол и 2,4-дихлороминдальная кислота). Метронидазол. Метаболизируется в печени путем окисления, гидроксильный метаболит является активным. Основные метаболиты метронидазола, гидроксильные и метаболиты уксусной кислоты, выделяются с мочой. Гидроксильный метаболит имеет 30% биологической активности метронидазола. Выведение Миконазола нитрат. Период полувыведения составляет 24 часа. Менее 1% выводится с мочой. Около 50% выводится с калом, обычно в неизмененном виде. Метронидазол. Период полувыведения составляет 6–11 часов. Около 6–15% дозы метронидазола выводится с калом, 60–80% не изменяется и выводится с мочой, как и его метаболиты. Около 20% метронидазола выводится с мочой в виде неизмененного вещества. Данные доклинических исследований Результаты стандартных доклинических исследований токсичности при многократном применении, генотоксичности, канцерогенности и репродуктивной токсичности не указывают на существование специфического риска для человеческого организма. В микробиологическом исследовании in vitro не было обнаружено синергического или антагонистического взаимодействия между действующими веществами, входящими в состав препарата, в отношении действия против Candida albicans, Streptococcus (грамм B по Lancefield), Gardnerella vajinalis и Trichomonas vaginalis. Доклинические исследования комбинации 750 мг метронидазола и 200 мг миконазола нитрата показали, что нет усиления или синергизма летальных или токсичных эффектов обоих составляющих у самок крыс. В исследовании раздражения слизистой оболочки влагалища у самок собак породы бигль той же комбинацией препаратов было определено, что она не вызывает раздражения слизистой оболочки влагалища и не приводит к клиническим, биохимическим и гематологическим нарушениям. В том же исследовании местных и системных токсических эффектов выявлено не было. Для лечения кандидозных вульвовагинитов, вызванных Candida albicans, бактериальных вагинозов, вызванных анаэробными бактериями и Gardnerella vaginalis, трихомонадных вагинитов, вызванных Trichomonas vaginalis, и смешанных вагинальных инфекций. Из-за абсорбции метронидазола могут наблюдаться реакции взаимодействия препарата при одновременном применении с некоторыми веществами и лекарственными средствами. Алкоголь: взаимодействие метронидазола с алкоголем может вызвать реакцию, аналогичную взаимодействию с дисульфирамом. Амиодарон: повышение риска кардиотоксичности (пролонгация интервала QT, трепетание-мерцание желудочков, остановка сердца). Астемизол и терфенадин: метронидазол подавляет метаболизм этих лекарств и увеличивает их концентрацию в плазме. Карбамазепин: увеличивается концентрация карбамазепина в крови. Циметидин: увеличивается уровень метронидазола в крови и риск возникновения неврологических побочных эффектов. Циклоспорин: повышается риск токсичности циклоспорина. Дисульфирам: эффекты со стороны центральной нервной системы (например, психотические реакции). Литий: увеличивается уровень в крови и токсичность лития. Фенитоин: увеличивается уровень фенитоина в крови, снижается уровень метронидазола в крови. Фенобарбитал: снижается уровень метронидазола в крови. Фторурацил: увеличивается уровень в крови и токсичность фторурацила. Пероральные антикоагулянты: усиливается действие антикоагулянтов. Во время лечения метронидазолом наблюдалось его влияние на уровень в крови ферментов печени, глюкозы (гексокиназный метод), теофиллина и прокаинамида. Из-за особенностей абсорбции миконазола нитрата при одновременном применении нижеприведённых лекарственных средств могут наблюдаться следующие реакции Аценокумарол, анисиндион, дикумарол, Фенидион, фенпрокумон, варфарин: повышение риска возникновения кровотечения. Астемизол, цизаприд и терфенадин: миконазол угнетает метаболизм этих лекарств и увеличивает их концентрацию в плазме. Карбамазепин: снижается метаболизм карбамазепина. Циклоспорин: повышается риск токсичности циклоспорина (дисфункция почек, холестаз, парестезии). Фентанил: увеличивается или пролонгируется действие опиоидов (угнетение центральной нервной системы, депрессия, угнетение дыхания). Фенитоин и фосфенитоин: увеличивается риск токсичности фенитоина (атаксия, гиперлексия, нистагм, тремор). Глимепирид: увеличивается гипогликемическое действие. Оксибутинин: увеличивается концентрация в плазме крови или действие оксибутинина. Оксикодон: увеличивается концентрация оксикодона в плазме крови и снижается его выведение. Пимозид: увеличивается риск кардиотоксичности (пролонгация интервала QT, трепетание-мерцание желудочков, остановка сердца). Толтеродин: увеличивается биодоступность толтеродина у лиц с недостаточностью действия цитохрома P450 2D6. Триметрексат: увеличение токсичности триметрексата (угнетение костного мозга, нарушение функции почек и печени и образование язв в желудке и кишечнике). Следует предупредить пациента о том, что нельзя употреблять алкоголь во время терапии и в течение 2 суток после завершения курса лечения из-за возможности возникновения реакций со стороны центральной нервной системы, аналогичных действию дисульфирама. Высокие дозы препарата и длительный срок применения могут вызвать периферическую нейропатию и судороги. Основа суппозитория может нежелательным образом взаимодействовать с резиной или латексом, из которых изготавливаются контрацептивные диафрагмы и презервативы, поэтому их одновременное применение с суппозиториями не рекомендуется. Половые партнеры пациентов с трихомонадным вагинитом также должны пройти курс лечения. При почечной недостаточности дозу метронидазола необходимо уменьшить. При тяжелой печеночной недостаточности может быть изменен клиренс метронидазола. Метронидазол может ухудшать симптомы энцефалопатии в связи с его повышенным уровнем в плазме крови. Таким образом, метронидазол необходимо применять с осторожностью пациентам с печеночной энцефалопатией. Суточную дозу для таких пациентов следует уменьшить до 1/3. Для пациентов пожилого возраста (старше 65 лет): такие же рекомендации, как и для остальных пациентов. Препарат не рекомендуется применять девственницам. Не следует глотать суппозитории или применять препарат любым другим путем введения. Беременность — категория C Так как эффекты действующих веществ препарата Нео-Пенотран® Форте на плод и развитие новорожденных до конца не изучены, женщинам, которым необходимо применять этот препарат, следует избегать беременности с помощью эффективного противозачаточного метода. Данные доклинических исследований на животных в отношении беременности, эмбрионального развития и развития плода, перинатального и/или постнатального развития недостаточны. Возможный риск для людей неизвестен. Данных о применении препарата Нео-Пенотран® Форте в первом триместре беременности недостаточно. Поэтому препарат Нео-Пенотран® Форте не следует применять в первом триместре беременности. Во втором и третьем триместрах препарат можно применять только в случае необходимости, если врач решит, что польза превышает риск. Нет доказательств опасного воздействия на фертильность людей и животных при применении отдельно метронидазола или миконазола нитрата. Во время применения препарата Нео-Пенотран® Форте следует прекратить кормление грудью, поскольку метронидазол, один из активных компонентов препарата, проникает в грудное молоко. Кормление грудью можно возобновить через 1–2 суток после окончания лечения. Системное применение метронидазола может влиять на управление автотранспортом или работу с другими механизмами. По сравнению с системным применением, при вагинальном введении абсорбция метронидазола значительно ниже. Существует возможность возникновения головокружения, атаксии, психоэмоциональных расстройств. При наличии таких симптомов не рекомендуется управлять автотранспортом или работать с другими механизмами. По 1 суппозиторию вагинальному следует вводить глубоко во влагалище на ночь в течение 7 дней. При рецидивах заболевания или вагинитах, резистентных к другому лечению, препарат Нео-Пенотран® Форте следует применять в течение 14 дней. Не рекомендуется применять Нео-Пенотран® Форте в период менструации из-за снижения эффективности препарата, возможность некоторых осложнений при введении. Препарат не рекомендуется применять детям. Нет данных о передозировке метронидазола при вагинальном введении у людей. При введении во влагалище метронидазол может всасываться в количестве, достаточном для того, чтобы вызвать системные эффекты. Если случайно в пищеварительную систему попадет большое количество препарата, в случае необходимости следует применить соответствующий метод промывания желудка. Лечение нужно проводить в случаях, когда в пищеварительную систему попало 12 г метронидазола. Специфического антидота не существует, рекомендуется симптоматическое лечение. При передозировке метронидазола наблюдаются такие симптомы: тошнота, рвота, боль в животе, диарея, зуд, металлический привкус во рту, атаксия, вертиго, парестезии, судороги, лейкопения, потемнение мочи. При передозировке миконазола нитрата наблюдаются такие симптомы: тошнота, рвота, воспаление горла и ротовой полости, анорексия, головная боль, диарея. Частота перечисленных ниже побочных явлений определяется следующим образом: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1.000 до <1/100), редко (от ≥1/10000 до <1/1.000) очень редко (<1/10.000), неизвестно (нельзя оценить по имеющимся данным). В отдельных случаях могут наблюдаться такие побочные эффекты как, реакции гиперчувствительности (в том числе высыпания на коже) и боль в брюшной полости, головная боль, зуд, жжение и раздражение влагалища. Частота возникновения системных побочных эффектов очень незначительная вследствие очень низкого уровня метронидазола в плазме крови при вагинальном применении препарата (2–12% от уровня, который достигается при пероральном применении метронидазола). Другое действующее вещество препарата, миконазола нитрат, может вызвать раздражение влагалища (жжение, зуд), как и все другие противогрибковые средства с содержанием производных имидазола, которые вводятся вагинально (2–6%). В случае возникновения тяжелого раздражения необходимо прекратить лечение. Побочные эффекты в результате системного действия действующих веществ Нео-Пенотран® Форте приведены ниже. Нарушения со стороны крови и лимфатической системы Неизвестно: лейкопения. Нарушения со стороны иммунной системы Неизвестно: реакции гиперчувствительности, аллергические реакции (в тяжелых случаях может развиться анафилактический шок). Психиатрические нарушения Нечасто: депрессия. Очень редко: нарушения сознания. Нарушения со стороны нервной системы Часто: головокружение, головная боль. Неизвестно: усталость или слабость, атаксия, судороги, периферическая нейропатия вследствие интенсивной и/или длительной терапии метронидазолом. Гастроинтестинальные нарушения Неизвестно: нарушение вкуса, металлический привкус, тошнота, рвота, запор, сухость во рту, диарея, снижение аппетита, боли в животе и спазмы. Общие нарушения и реакции в месте введения Очень часто: вагинальные выделения. Часто: вагинит, вульвовагинальное раздражение, дискомфорт в области малого таза. Нечасто: ощущение жажды. Редко: жжение во влагалище, зуд, раздражение, боли в желудке, сыпь. Неизвестно: местное раздражение и гиперчувствительность, контактный дерматит. Названные побочные эффекты наблюдаются редко, поскольку концентрация метронидазола в крови при интравагинальном введении невысока. 2 года. Хранить при температуре не выше 25 °С, в местах, недоступных для детей. Препарат можно хранить в холодильнике при температуре 2–8 °С. Не замораживать. Одна упаковка содержит 7 суппозиториев вагинальных. По рецепту. Эмбил Фармацеутикал Ко. Лтд., Турция./ Embil Pharmaceutical Co. Ltd., Turkey. Tekirdag province, Cerkezkoy district, Cerkezkoy Organize Sanayi Bolgesi, Gaziosmanpasa Mah., Fatih Bulvari, № 19/2, Turkey. Провинция Текирдаг, район Черкезкой, Черкезкой Органайз Санаи Бельгесе, Газиосманпаша Мах., бульвар Фати, № 19/2, Турция.ИНСТРУКЦИЯ
по медицинскому применению препарата
НЕО-ПЕНОТРАН® ФОРТЕ
(NEO-PENOTRAN® FORTE)
Состав:
Лекарственная форма.
Фармацевтические характеристики.
Фармакотерапевтическая группа.
Фармакологические свойства.
Клинические характеристики.
Показания.
Противопоказания.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий.
Особенности применения.
Применение в период беременности или кормления грудью.
Способность влиять на скорость реакции при управлении автотранспортом или работе с другими механизмами.
Способ применения и дозы.
Дети.
Передозировка.
Побочные реакции.
Срок годности.
Условия хранения.
Упаковка.
Категория отпуска.
Производитель.
Местонахождение.